Flagship products where clinical needs, AI, and user workflows converge. 임상 요구, AI, 사용자 워크플로가 하나로 수렴하는 프로덕션 제품들.
Canopus SW · Patented MSI diagnostic system with clinical deployment Canopus SW · 특허 MSI 진단 시스템 — 임상 배포 완료
My role담당 역할
Project Lead & AI Engineer: Owned the complete product lifecycle — clinical requirement gathering (pathologist interviews), system architecture design, AI model development (>0.99 AUC), C#–Python integration, systematic software development design in accordance with IEC 62304, considering CE-IVDR/FDA/MFDS (Korea Regulatory) requirements, and production deployment. 프로젝트 리드 & AI 엔지니어: 병리학자 인터뷰를 통한 임상 요구사항 수집, 시스템 아키텍처 설계, AI 모델 개발(>0.99 AUC), C#–Python 통합, CE-IVDR/FDA/MFDS (Korea Regulatory) 요구사항을 고려한 IEC 62304에 따른 체계적인 소프트웨어 개발 설계, 프로덕션 배포까지 전체 제품 주기를 책임졌습니다.
Problem문제
MSI detection from digital PCR melting data: unreliable in research, absent in production. Clinical labs need certified system: data analysis + AI scoring + operator review + PDF export, all meeting strict regulatory/security standards. 디지털 PCR 멜팅 데이터의 MSI 검출: 연구에서 신뢰성 낮음, 프로덕션 부재. 임상실험실 필요: 데이터 분석 + AI 스코어링 + 운영자 검토 + PDF 내보내기 + 규제/보안 기준 충족.
Solution해결책
3-layer architecture: C# UI (workflows) · C# signal processing (PCR/melting) · Python AI (patented Tm extraction + MSI scoring). Medical-grade security: encryption, access control, audit trails, compliance docs. 3계층 구조: C# UI(워크플로) · C# 신호 처리(PCR/멜팅) · Python AI(특허 Tm 추출 + MSI 스코어링). 의료 등급 보안: 암호화, 접근 제어, 감사 추적, 준수 문서.
C# UI LayerC# UI 레이어
Sample management · MSI score visualization · Threshold interpretation · Operator review workflow · PDF export with audit trails.샘플 관리 · MSI 점수 시각화 · 임계값 해석 · 운영자 검토 · 감사 추적 PDF 내보내기.
C# Analysis EngineC# 분석 엔진
Digital PCR + melting curve analysis · Preprocessing · Tm distribution modeling · QA checks · AI-ready data structures.PCR + 멜팅 커브 분석 · 전처리 · Tm 분포 모델링 · QA 확인 · AI 준비 데이터.
Python AI ModulePython AI 모듈
Patented Tm feature extraction · ML-based MSI-H scoring · Confidence metrics · Model validation.특허 Tm 특성 추출 · ML 기반 MSI-H 스코어링 · 신뢰도 지표 · 모델 검증.
Impact & Achievement성과 & 달성
- Patented core algorithms특허 핵심 알고리즘 — 2–10× signal resolution improvement over existing methods기존 방법 대비 2–10× 신호 해상도 향상
- >0.99 AUC — production-grade MSI classification on clinical cohorts임상 코호트에서 프로덕션 등급 MSI 분류 달성
- CE-IVDR/MFDS complianceCE-IVDR/MFDS 규제 준수 — complete certification pathway with encrypted data, audit trails, and security documentation암호화 데이터, 감사 추적, 보안 문서화를 포함한 완전한 인증 경로
- Currently deployed in pathology labs병리학 실험실 현재 배포 운용 중 — clinicians report improved workflow efficiency and result confidence임상의들이 워크플로 효율성과 결과 신뢰도 향상을 보고
Engineering excellence엔지니어링 특징
Clinical requirements shaped architecture; patented innovations enabled superior AI performance; seamless C#–Python integration proved robust in production; comprehensive regulatory documentation supports lab adoption and compliance audit. 임상 요구사항이 아키텍처를 결정했고, 특허 혁신이 우월한 AI 성능을 가능하게 했으며, 원활한 C#–Python 통합이 프로덕션에서 견고성을 증명했고, 포괄적인 규제 문서화가 실험실 도입과 컴플라이언스 감사를 지원합니다.
Dashboard and result review대시보드 및 결과 검토
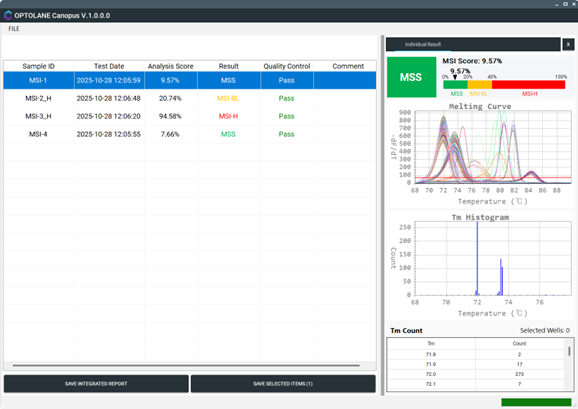
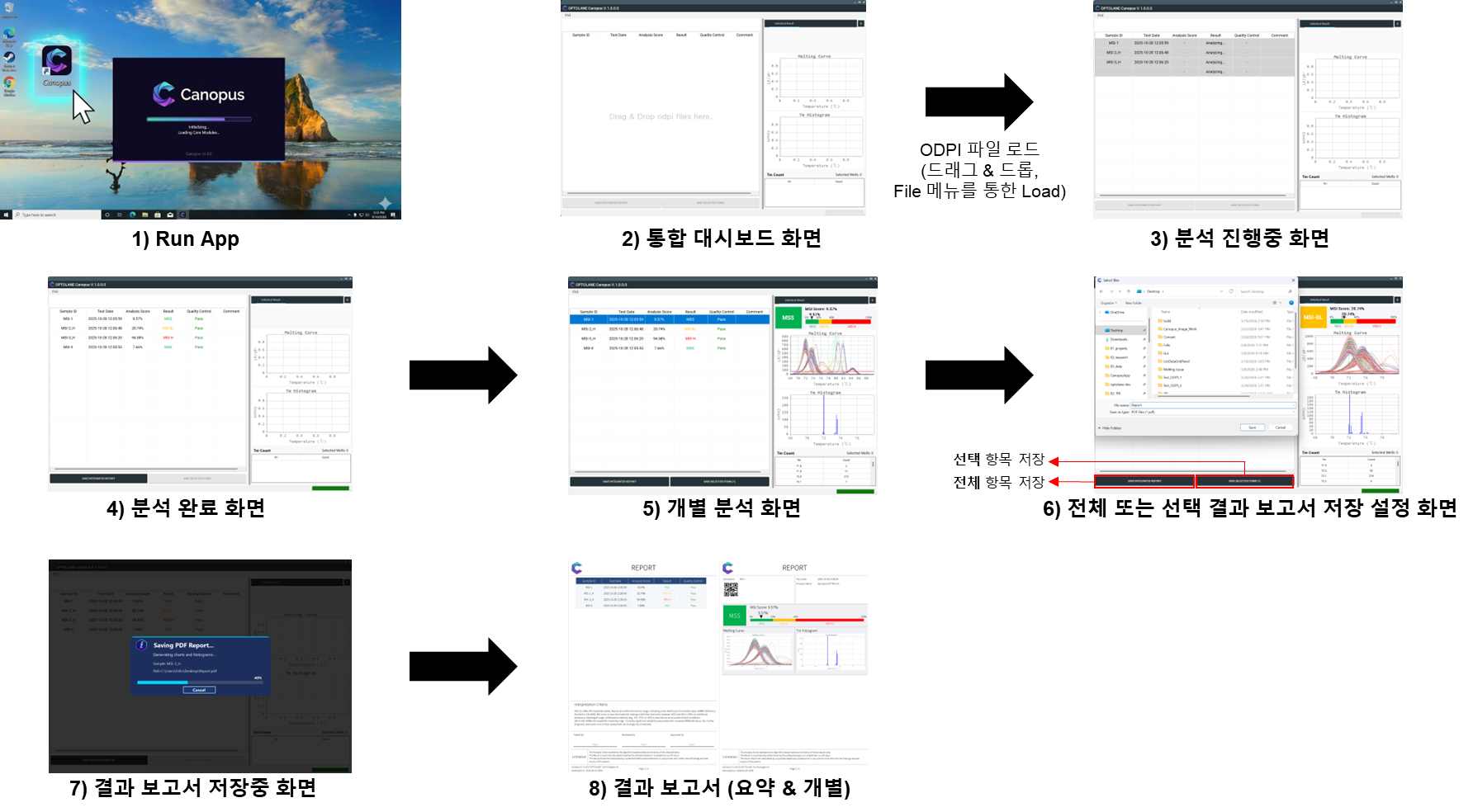
UI scenario and workflow overviewUI 시나리오 및 워크플로 개요
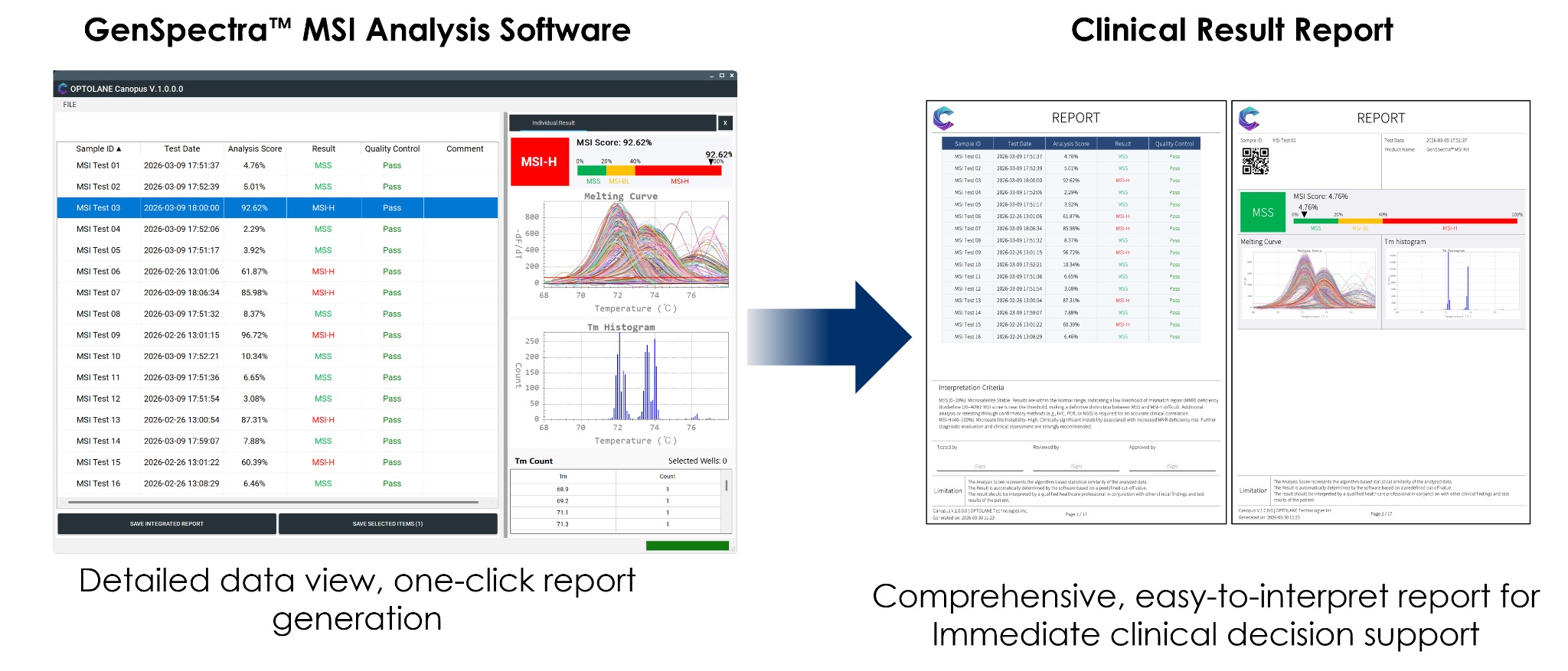
Application role and report output애플리케이션 역할 및 보고서 출력
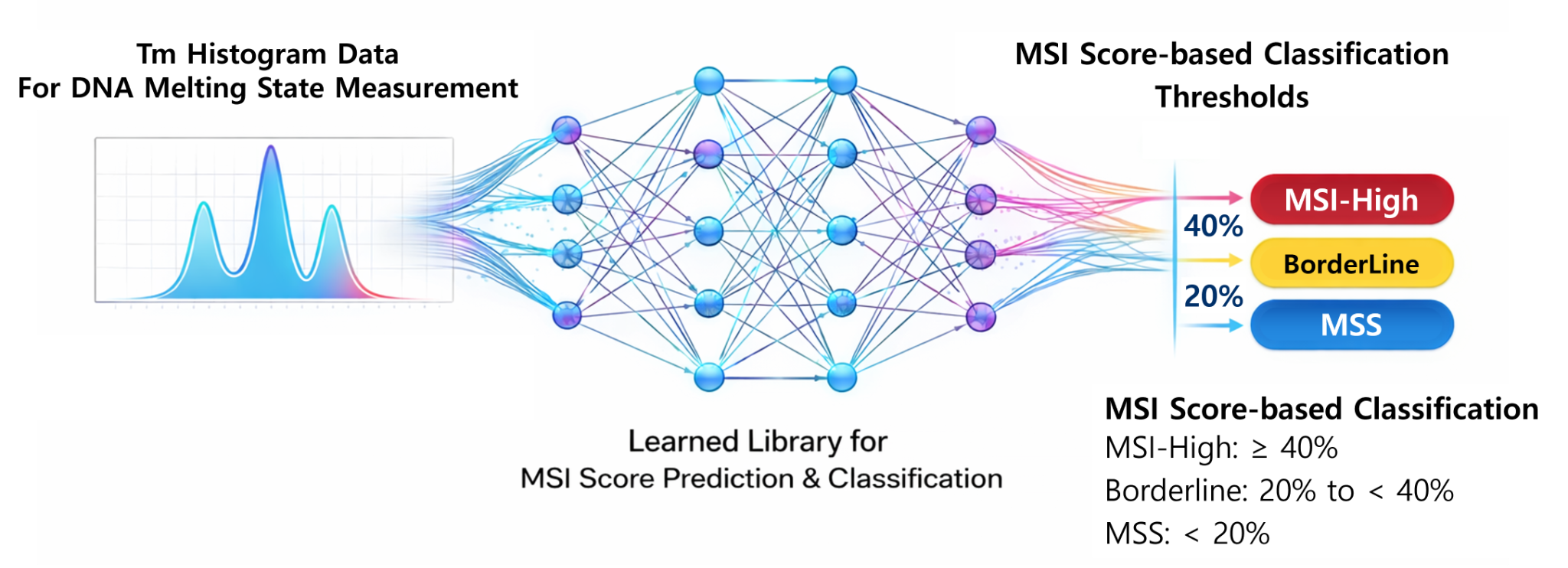
MSI score prediction modelMSI 점수 예측 모델
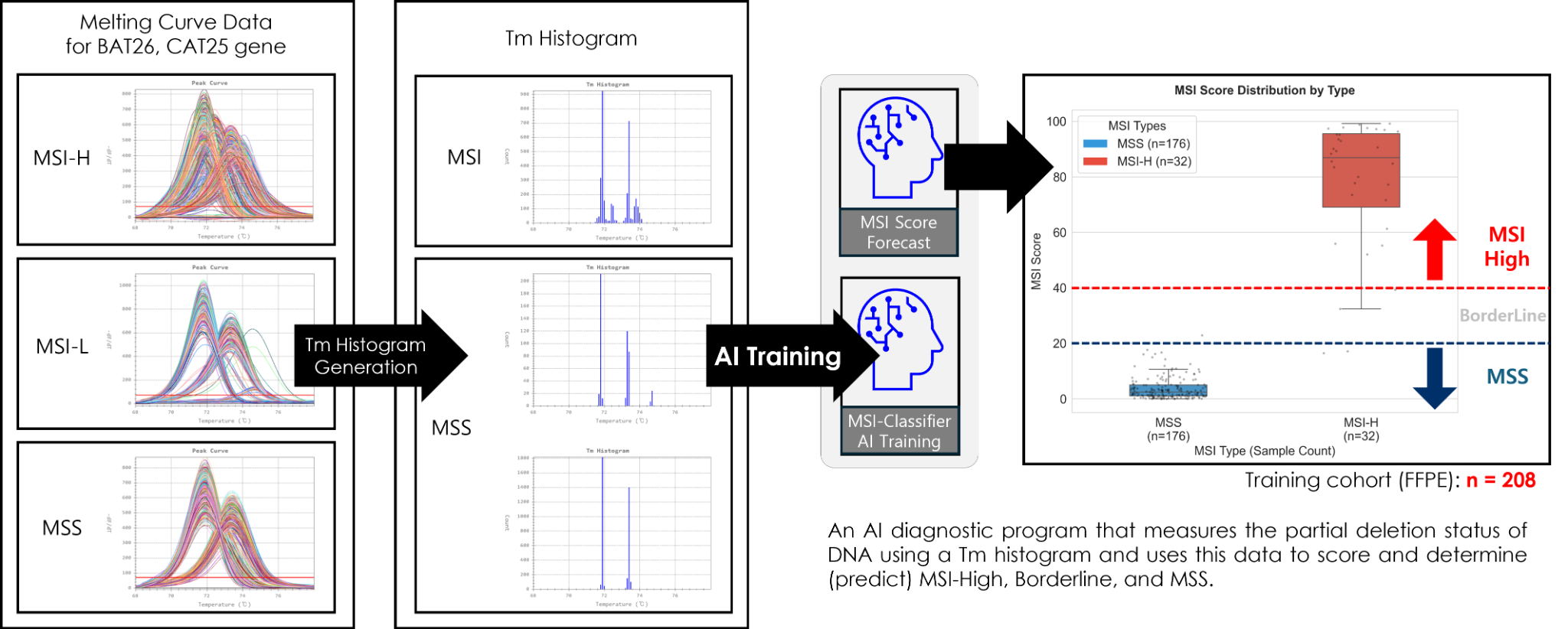
MSI classifier performanceMSI 분류기 성능
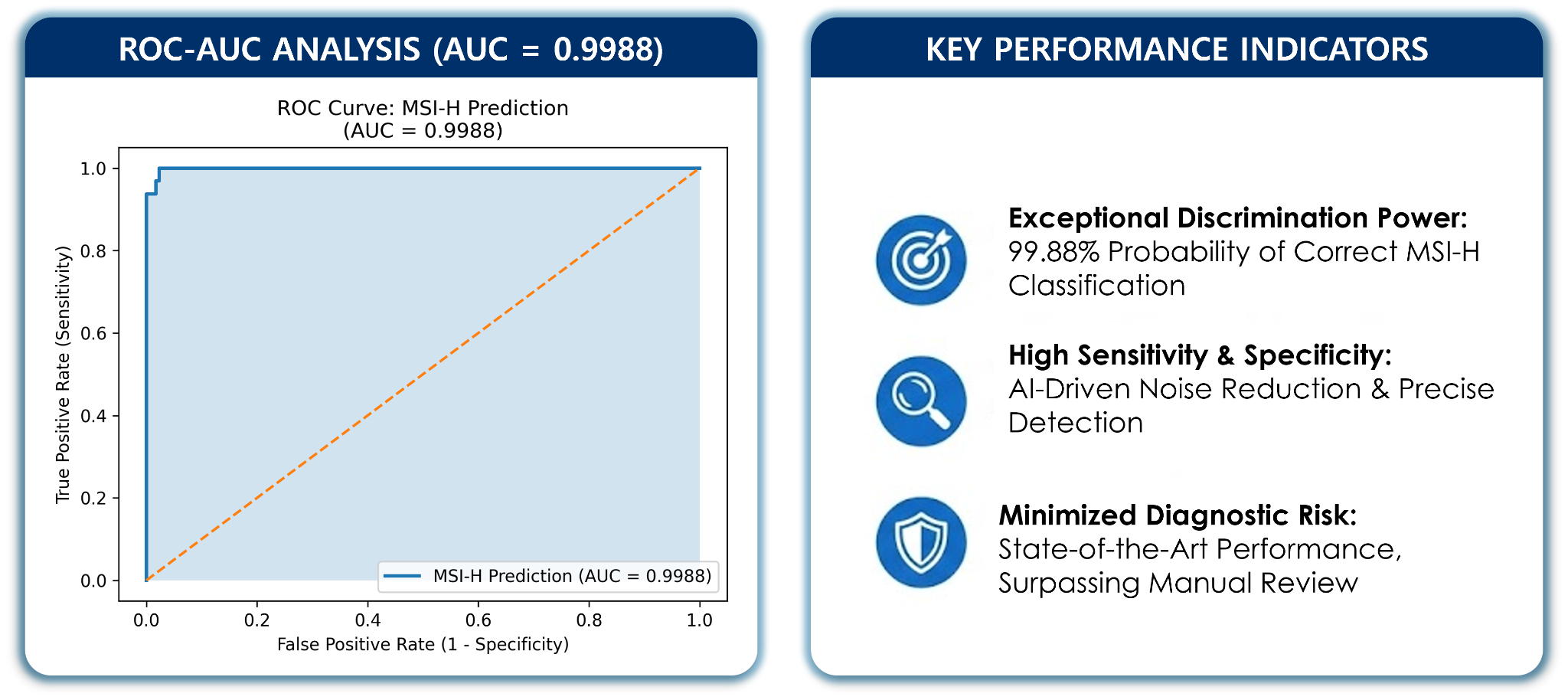
Classification pipeline and threshold interpretation분류 파이프라인 및 임계값 해석
CGT AI Pipeline · Automating cell therapy quality analysis CGT AI 파이프라인 · 세포 치료제 품질 분석 자동화
Background배경
Cell Gene Therapy (CGT) uses viral vectors to deliver genetic material into individual cells. To assess whether this delivery worked — and at what potency — researchers need to know how many viral copies entered each cell. This is measured through Cell Number Variation (CNV) analysis: a metric that requires correlating each cell's count with its corresponding PCR signal in the same reaction zone. 세포 유전자 치료(CGT)는 바이러스 벡터를 이용해 개별 세포에 유전 물질을 전달합니다. 이 전달이 효과적으로 이루어졌는지, 그 효능이 어느 정도인지 평가하려면 각 세포에 바이러스 복제물이 몇 개나 침투했는지를 알아야 합니다. 이를 Cell Number Variation(CNV) 분석이라 하며, 각 반응 구역(well)의 세포 수와 동일 구역의 PCR 신호를 정밀하게 연동해야 측정됩니다.
Problem문제
Counting cells in each reaction well requires a researcher to manually inspect dozens of microscope images — a process that is slow, subject to operator bias, and impossible to scale for clinical throughput. Without accurate, automated cell counts, CNV analysis cannot reliably quantify viral transduction efficiency or assess cell therapy quality. 각 반응 구역의 세포를 계수하려면 연구자가 수십 장의 현미경 이미지를 수작업으로 검토해야 합니다. 이는 느리고 운영자에 따라 결과가 달라지며 임상 수준의 처리량에 대응할 수 없습니다. 정확하고 자동화된 세포 계수 없이는 바이러스 침투 효율 측정이나 세포 치료제 품질 평가에서 CNV 분석의 신뢰성을 확보하기 어렵습니다.
Solution해결책
An automated dual-track pipeline that simultaneously processes optical microscope images and digital real-time PCR measurements. The system maps each reaction zone precisely using a pre-designed well layout, separates individual well images, counts cells with a deep learning model, then integrates the results with PCR data — delivering per-well CNV values fully automatically. 광학 현미경 이미지와 디지털 실시간 PCR 측정값을 동시에 처리하는 자동화 이중 트랙 파이프라인입니다. 사전 설계된 웰 레이아웃을 기반으로 각 반응 구역의 위치를 정밀하게 매핑하고, 개별 웰 이미지를 분리한 뒤, 딥러닝 모델로 세포를 계수하고, 이를 PCR 데이터와 연동해 웰별 CNV 값을 완전 자동으로 도출합니다.
Why it matters임상적 중요성
- Viral transduction efficiency — quantifies exactly how many viral copies entered each individual cell, the key metric in cell therapy potency assessment바이러스 침투 효율 — 개별 세포에 침투한 바이러스 복제물 수를 정밀 정량화, 세포 치료제 효능 평가의 핵심 지표
- Cell therapy quality control — enables reliable, operator-independent evaluation of whether the gene delivery worked at the single-cell level세포 치료제 품질 관리 — 단일 세포 수준에서 유전자 전달 성공 여부를 운영자 편향 없이 신뢰성 있게 평가
- >99.5% cell recognition accuracy — deep learning replaces manual counting with objective, reproducible results at any scale>99.5% 세포 인식 정확도 — 딥러닝이 수작업 계수를 대체, 어떤 규모에서도 객관적이고 재현 가능한 결과 제공
- Full prototype delivered in 2 months — end-to-end system including UI and analysis functions2개월 내 완전한 프로토타입 납품 — UI 및 분석 기능을 포함한 엔드투엔드 시스템
How CNV Analysis Works — Three-Stage OverviewCNV 분석 작동 원리 — 3단계 개요
Well Localization웰 위치 파악
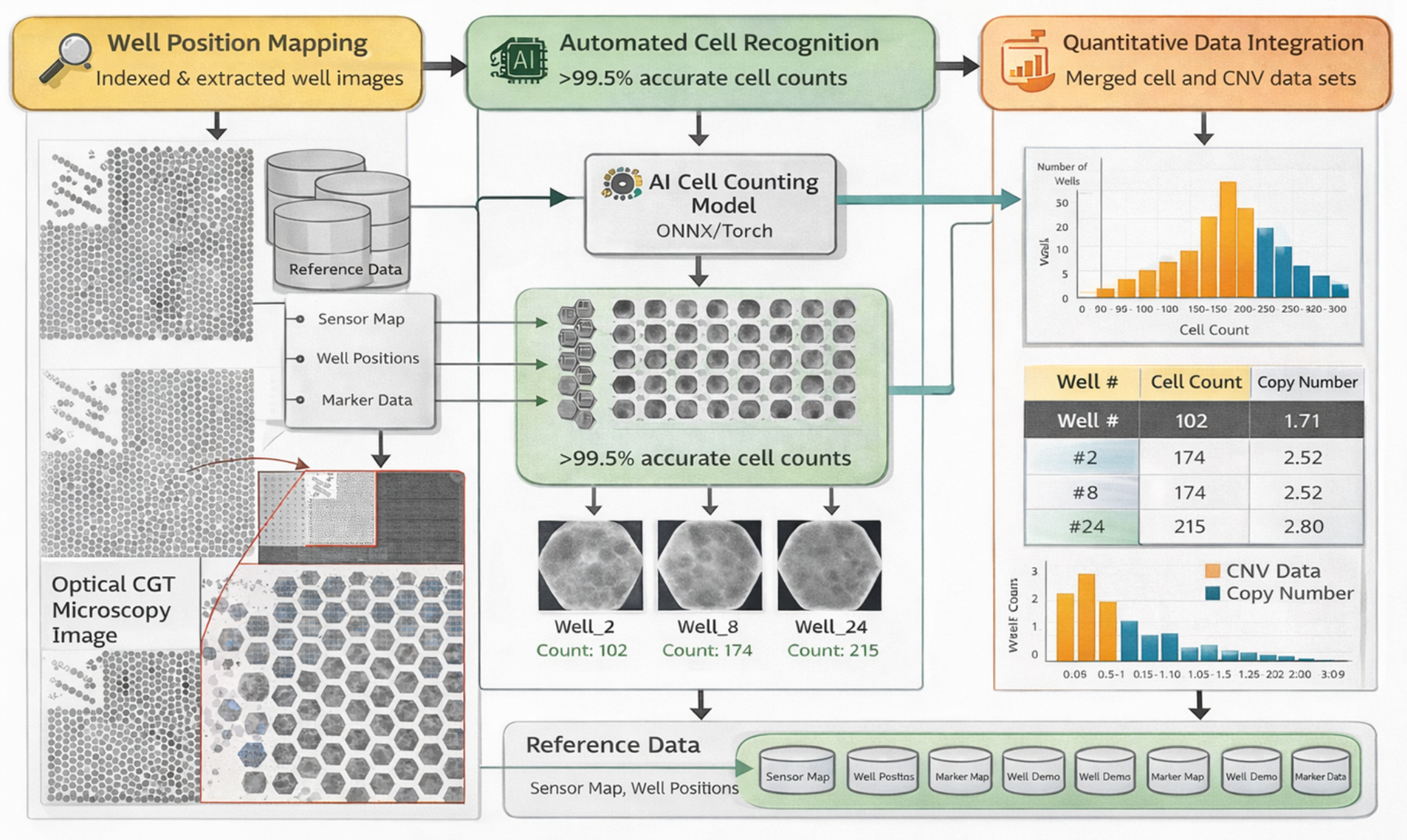
A pre-designed well grid map is used to precisely locate each reaction zone within the microscope image. Each well is then separated as an individual image for downstream analysis. 사전 설계된 웰 격자 맵으로 현미경 이미지 내 각 반응 구역의 위치를 정밀하게 파악합니다. 이후 각 웰을 개별 이미지로 분리하여 다음 단계에서 분석합니다.
AI Cell CountingAI 세포 계수
A deep learning model automatically identifies and counts every cell within each separated well image — replacing manual microscope counting with objective, reproducible results. 딥러닝 모델이 분리된 각 웰 이미지에서 모든 세포를 자동으로 감지하고 계수합니다. 수작업 현미경 계수를 객관적이고 재현 가능한 결과로 대체합니다.
CNV AnalysisCNV 분석
Cell count per well is matched with the PCR signal from the same well, revealing how many viral gene copies entered each cell. 웰별 세포 수를 동일 웰의 PCR 신호와 매칭하여 각 세포에 몇 개의 바이러스 유전자 복제물이 침투했는지 측정합니다.
| Well웰 | Cell Count세포 수 | CNV |
|---|---|---|
| #2 | 102 | 1.71 |
| #8 | 174 | 2.52 |
| #24 | 215 | 2.80 |
Automated Pipeline — How the two data sources are unified자동화 파이프라인 — 두 데이터 소스의 통합 과정
Using the well grid map, identify exactly where each reaction zone is in the microscope image and extract it as an individual image.웰 격자 맵으로 현미경 이미지 내 각 반응 구역의 위치를 특정하고 개별 이미지로 추출합니다.
Extract and process the PCR amplification signal from each individual reaction zone to quantify gene copy numbers.각 반응 구역의 PCR 증폭 신호를 추출하고 처리하여 유전자 복제 수를 정량화합니다.
A deep learning model detects and counts every cell within each separated well image — automatically and objectively.딥러닝 모델이 분리된 각 웰 이미지 내 모든 세포를 자동으로 감지하고 객관적으로 계수합니다.
Align PCR signal data with the spatially indexed well positions so every well's signal corresponds to the correct reaction zone.PCR 신호 데이터를 공간적으로 인덱싱된 웰 위치와 정렬하여 모든 웰의 신호가 올바른 반응 구역에 대응하도록 합니다.
Cell count per well is combined with the PCR signal from the same well to compute the CNV value — the number of viral gene copies per cell. This directly measures how effectively the viral vector delivered its genetic cargo into individual cells.웰별 세포 수와 동일 웰의 PCR 신호를 결합하여 CNV 값, 즉 세포당 바이러스 유전자 복제 수를 산출합니다. 이는 바이러스 벡터가 개별 세포에 유전적 화물을 얼마나 효과적으로 전달했는지를 직접 측정하는 지표입니다.
LOAA-M · Diagnostic PCR Platform — Qt UI, AWS integration & cybersecurity LOAA-M · 진단 PCR 플랫폼 — Qt UI, AWS 연동 & 사이버 보안
What it is제품 개요
LOAA-M is OPTOLANE's molecular diagnostic PCR instrument platform for clinical laboratories. The software stack drives real-time diagnostic data acquisition, analysis, cloud synchronization, and secure data management — operating in certified medical environments across Linux and Windows. LOAA-M은 임상 실험실을 위한 OPTOLANE의 분자 진단 PCR 기기 플랫폼입니다. 소프트웨어 스택은 실시간 진단 데이터 수집, 분석, 클라우드 동기화, 보안 데이터 관리를 담당하며 Linux 및 Windows 인증 의료 환경에서 운용됩니다.
My contributions담당 역할
Qt Desktop UIQt 데스크톱 UI
Led development of the full Qt-based operator UI for Linux and Windows. Designed real-time diagnostic data visualization, instrument control screens, and result review workflows optimized for clinical lab operators.Linux 및 Windows용 Qt 기반 운영자 UI 전체 개발을 주도했습니다. 실시간 진단 데이터 시각화, 기기 제어 화면, 임상 실험실 운영자에 최적화된 결과 검토 워크플로를 설계했습니다.
AWS Network IntegrationAWS 네트워크 연동
Built cloud data integration connecting LOAA-M instruments to AWS servers using Java on Windows. Implemented secure diagnostic data upload, retrieval, and multi-site synchronization across networked laboratory environments.Java를 사용하여 LOAA-M 기기와 AWS 서버를 연결하는 클라우드 데이터 연동을 구축했습니다. 보안 진단 데이터 업로드, 조회, 네트워크 연결 실험실 환경에서의 다중 사이트 동기화를 구현했습니다.
Cybersecurity Architecture사이버 보안 아키텍처
Designed and implemented the medical-grade security stack: equipment and network communication encryption, database access control with role-based permissions, and stored data encryption — fully compliant with CE-IVDR and MFDS cybersecurity requirements.의료 등급 보안 스택을 설계하고 구현했습니다: 기기·네트워크 통신 암호화, 역할 기반 권한의 데이터베이스 접근 제어, 저장 데이터 암호화 — CE-IVDR 및 MFDS 사이버 보안 요건을 완전히 충족합니다.
Impact & Achievement성과 & 달성
- Cross-platform Qt UI deployed on both Linux and Windows clinical environments with stable long-term operation크로스 플랫폼 Qt UI — Linux 및 Windows 임상 환경 모두에 배포, 안정적 장기 운용 중
- AWS cloud integration enabling multi-site diagnostic data sharing and remote result accessAWS 클라우드 연동 — 다중 사이트 진단 데이터 공유 및 원격 결과 접근 가능
- End-to-end encryption across device, network, and database layers meeting medical device security standards엔드투엔드 암호화 — 기기·네트워크·데이터베이스 레이어 전반에 걸쳐 의료기기 보안 기준 충족
- CE-IVDR and MFDS certification documentation prepared covering UI scenarios, security architecture, and data managementCE-IVDR 및 MFDS 인증 문서 작성 — UI 시나리오, 보안 아키텍처, 데이터 관리 망라
- MariaDB optimization for high-throughput diagnostic data storage with secure access controls and performance tuningMariaDB 최적화 — 고처리량 진단 데이터 저장, 보안 접근 제어, 성능 튜닝
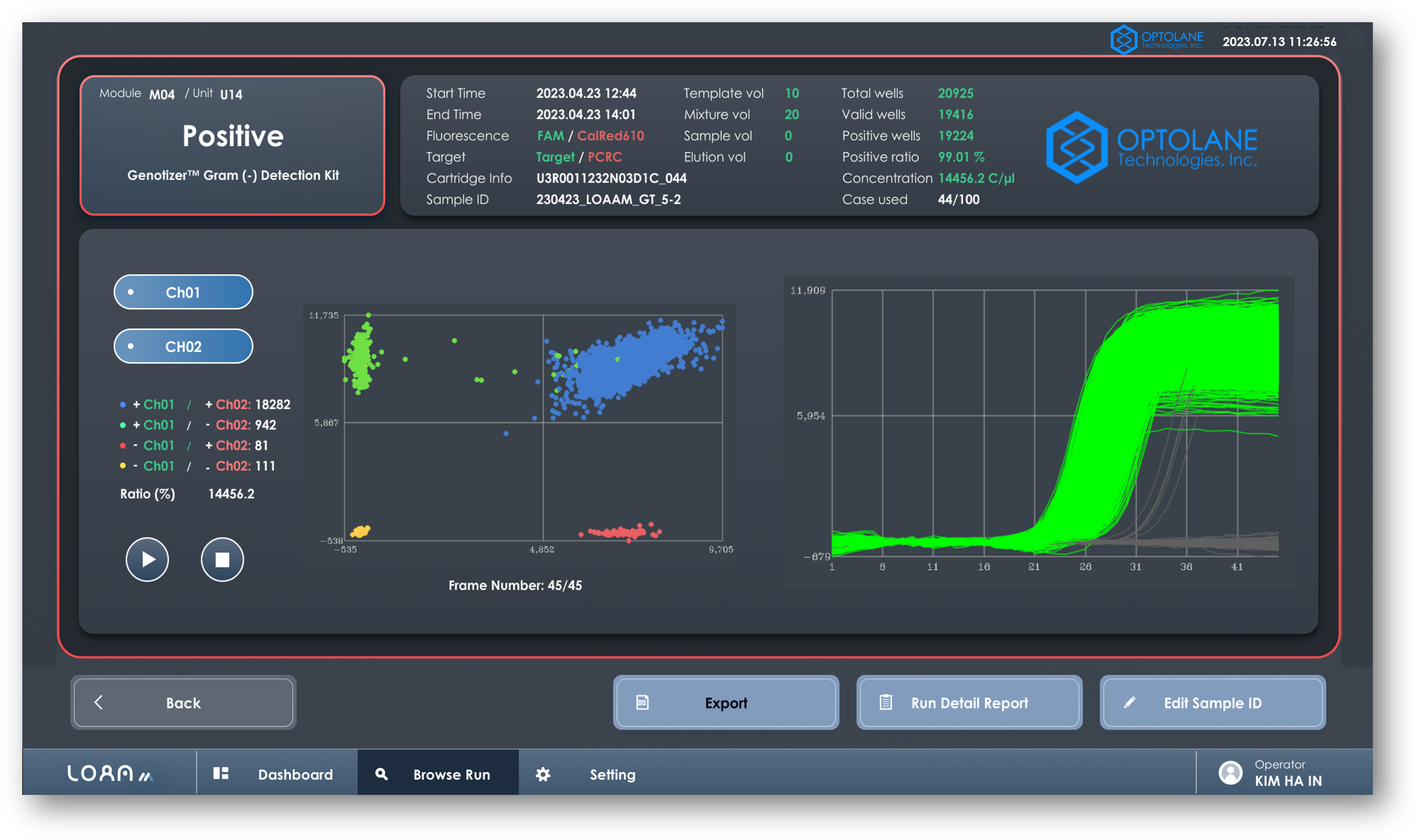
LOAA-M PCR Instrument — Clinical deploymentLOAA-M PCR 기기 — 임상 배포

Qt UI — Real-time diagnostic interfaceQt UI — 실시간 진단 인터페이스
Deep Learning Breast Cancer Targeting Model 딥러닝 기반 유방암 표적화 모델
Objective목표
Develop a deep learning model for breast cancer prediction, applying advanced targeting techniques to push accuracy beyond baseline EfficientNet-B2 performance.딥러닝 기반 유방암 예측 모델을 개발하고, 고급 표적화 기법을 적용하여 기준 EfficientNet-B2 성능 이상의 정확도를 달성했습니다.
Approach & Result접근법 & 결과
- Designed breast cancer prediction model based on EfficientNet-B2, achieving initial accuracy of 86%EfficientNet-B2 기반 유방암 예측 모델 설계, 초기 정확도 86% 달성
- Applied probability-density–based targeting enhancement techniques to improve model focus on high-risk regions확률 밀도 기반 표적화 향상 기법 적용으로 고위험 영역에 대한 모델 집중도 향상
- Improved accuracy to 93% — a 7 percentage-point gain through targeted enhancement표적화 향상을 통해 정확도를 93%로 개선 — 7%p 향상